Formula empirica e formula molecolare
Come si è visto nel calcolo percentuale, la conoscenza della formula chimica del composto è indispensabile ai fini dello svolgimento dei vari calcoli. Ci si può allora chiedere come sia possibile ottenere la formula chimica di una data sostanza.
Come tutte le principali informazioni che si usano in chimica, anche la
formula di un composto deriva da dati sperimentali, usualmente raccolti
in laboratorio. Quando si ha a che fare con un composto incognito, i chimici
determinano quali tipi di atomi sono presenti tramite l'analisi qualitativa,
calcolando poi la percentuale in massa dei vari elementi appartenenti al
composto tramite l'analisi quantitativa.
Questi calcoli portano alla formula empirica del composto.
La formula empirica o formula minima di un composto, indica il minimo rapporto tra gli atomi degli elementi che formano quel composto.
Poi una informazione supplementare, sempre ottenuta per via sperimentale, la massa molecolare del composto, permette di convertire la formula empirica in formula molecolare.
La formula molecolare di un composto indica quanti atomi di ciascun elemento sono presenti in una molecola di quella sostanza.
Per calcolare la formula empirica di un composto si esegue la seguente procedura:
a Si fa riferimento a 100g di composto, di conseguenza le percentuali si possono esprimere in grammi.
b Si converte la massa in grammi di ciascun elemento nelle moli di atomi di quell'elemento.
c Si dividono le moli di ciascun elemento per il valore più piccolo (di moli ottenute) per trovare i rapporti molari.
d I numeri interi che vengono ottenuti costituiscono gli indici degli elementi della formula empirica (formula minima).
La formula molecolare indica il numero reale di atomi di ciascun elemento in una molecola di sostanza.
Per convertire la formula empirica in formula molecolare è necessario determinare, per via sperimentale, la massa molecolare (PM) del composto, poi si eseguono i seguenti passaggi:
a Si calcola la massa della formula empirica.
b Si ottiene un numero intero n
![]()
c Si moltiplica la formula empirica per n.
Esempio : la nicotina è un composto organico contenente carbonio, idrogeno e ossigeno in percentuali: C,74,03%; H 8,70% ; N 17,27%. La determinazione della massa molecolare ha dato come risultato 162,1 g/mol. determinare la formula molecolare della nicotina.
Si deduce che su 100 g di sostanza ci sono
74,03g di C con PM(C)=12,01 g/mol
8,7g di H con PM(H)=1,01 g/mol
17,27g di N con PM(N)=14,01 g/mol
sempre su 100g di nicotina avremo
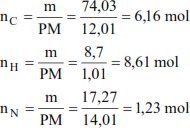
dividiamo i tre risultati ottenuti per il risultato più piccolo, ottenendo
![]()
si deduce un rapporto tra le moli di C,H,N pari a 5,7,1 dunque la formula
empirica della nicotina è C5H7N.
Determiniamo il coefficiente n considerando la massa della formula empirica:
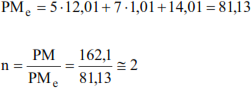
moltiplicando per 2 gli indici di ciascun elemento nella formula minima,
si ottiene che la formula molecolare della nicotina è:
(C5H7N)2 = C10H14N2.
 edutecnica
edutecnica